[0:01]Bien, nous allons quitter le rein pour monter vers le cerveau. Et je vais vous présenter en quelques mots le professeur Laurent Nguyen qui est notre prochaine orateur. Il est docteur en sciences biomédicales expérimentales et chercheur qualifié du FRS FRS. Après avoir réalisé une thèse de doctorat en neurobiologie du développement sous la direction de notre second vice-président le professeur Gustave Mouin à l'ULG, il a décroché une bourse de recherche MBO pour effectuer un stage postdoctoral dans le laboratoire du docteur François Guimot au National Institute for Medical Research à Londres. Il a également séjourné au Canada dans le laboratoire du docteur Carole Schuman à l'Université de Calgary. Actuellement, le docteur Guyenne dirige le laboratoire de régulation moléculaire de la neurogénèse au Giga neurosciences à Liège. Et avec son groupe, il étudie les mécanismes cellulaires et moléculaires qui régissent la formation du cortex cérébral. Je il est l'auteur bien sûr de nombreuses publications de haut niveau. Il a été récompensé de nombreux prix. Le dernier lui a été remis par son altesse royale la princesse Astrid puisqu'il a reçu tout récemment le prix Simone et Pierre Clerdent qui lui a été remis à Cologne il y a quelques semaines. C'est donc avec plaisir que je lui passe la parole et il va nous parler de migration neuronale dans le cortex cérébral en développement. Monsieur Guyenne, à vous. Merci monsieur le président, monsieur le secrétaire perpétuel, chers confrères. C'est un grand plaisir d'être là aujourd'hui et un honneur. J'aimerais vous parler aujourd'hui de travaux réalisés au sein de mon laboratoire qui ont trait au contrôle moléculaire de la migration neuronale dans le cortex cérébral pendant le développement. Comme vous le savez, le cortex correspond à l'écorce du cerveau et chez l'homme, mesure une épaisseur de quelques millimètres. Cette structure est divisée en différentes régions, appelées lobes. Parmi lesquels on retrouve des zones fonctionnelles, comme le cortex moteur primaire, le cortex somatosensoriel, des aires importantes pour l'audition, pour la vision, l'olfaction, encore le langage. Les autres régions font partie de ce qu'on appelle le cortex associatif. Une coupe coronale à travers cette structure nous permet d'apprécier l'histologie du cortex. Vous avez ici deux demi-sections à travers le cerveau de l'homme ou de la souris. Cette petite région représente une partie du cortex. Le cortex est une structure laminaire. Il est composé par des couches successives de neurones, six couches. Et les neurones qui appartiennent à la même couche partagent dans une certaine mesure des caractéristiques moléculaires et physiologiques.
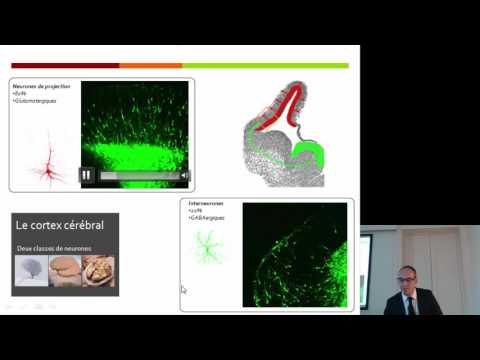
[3:32]De nos jours nous savons qu'il existe une multitude de différents types, de différentes classes de neurones que je diviserai en neurones excitateurs et neurones inhibiteurs. Pendant le développement embryonnaire, chez l'homme, mais également chez la souris, ces neurones naissent à partir des régions dites périventriculaire. Là où se trouve des cellules souches et progénitrices qui génèrent des vagues successives de neurones. La plupart des neurones sont les neurones excitateurs en vert ici. Ce sont des neurones de projection qui utilisent le glutamate comme neurotransmetteur principal. Il naissent localement dorsalement dans le cerveau antérieur à partir de ces cellules souches dont je vous ai parlé. Il migre ensuite une distance relativement courte par migration de type radiaire et s'installent dans les différentes couches du neurone du du cortex pardon. Ce sont des neurones de projection donc ils ont des axones qui projettent à distance dans le cortex ou dans des régions souscorticales comme la moelle épinière. 20 % des neurones les neurones restant du cortex sont des interneurones inhibiteur, nés dans la partie ventrale du cerveau antérieur, appelé éminence ganglionnaire. Ces neurones migrent de longue distance selon des chemins tangentiels pour atteindre le mur cortical en développement et s'intégrer localement dans des réseaux. Il s'agit de neurones inhibiteurs qui utilisent le GABA comme neurotransmetteur principal. Et donc il existe une balance excitation inhibition qui est importante pour le bon fonctionnement du cortex et dans certaines maladies caractérisées par exemple par de l'épilepsie, et bien il y a parfois un déficit d'inhibition parce que ces neurones par exemple ne sont pas produits correctement ou ne s'intègrent pas ou ne se différencient pas de façon adulte dans la structure. Finalement, on peut faire un parallélisme entre le programme génétique du développement du cortex avec le plan de l'architecte. En effet, si une erreur se glisse dans le plan, une erreur de dessin se glisse dans le plan, on peut avoir des problèmes de stabilité et aboutir par exemple à l'effondrement du bâtiment. Finalement, des mutations de gènes importants pour le contrôle de la mise en place des structures du cortex cérébral peuvent également aboutir à des malformations corticales qui sous-tendent des maladies neurologiques. Voici par exemple la lissencéphalie. En effet, je vous ai montré que l'aspect du cortex est plissé, il y a des circonvolutions chez l'homme, et bien dans cette maladie le cortex est lisse. Et vous voyez ici également un élargissement des ventricules et nous savons que chez ces patients, souvent, il y a des mutations dans des gènes qui codent pour des protéines importantes pour la régulation de la migration des neurones. Une autre malformation assez fréquente, relativement fréquente est la microcéphalie. Microcéphalie, le patient présente évidemment une réduction de la circonférence de de sa tête, mais également une réduction majeure de la taille du cerveau qui toutefois conserve une architecture globale conservée. Nous savons que parmi les microcéphalies primaires à caractère héréditaire, il y a des mutations qui touchent des gènes importants pour le contrôle soit de la production des neurones. Il y a moins de neurones générés par les cellules souches ou par la survie. En fait, ces neurones générés ne survivent pas correctement, il y a donc un déficit neuronal important qui crée cette microcéphalie chez l'homme. Au laboratoire, nous utilisons principalement comme modèle animal la souris. nous couplons également ces études avec des études réalisées sur des cellules souches pluripotentes induites humaines. Mais je vous parlerai aujourd'hui des des souris. Alors pourquoi la souris ? Parce que c'est bien sûr un un modèle où on peut facilement ou relativement facilement manipuler l'expression des gènes. Le temps de gestation est rapide, ce qui nous permet d'avoir accès euh à des embryons. Et le développement cortical est relativement proche de celui de l'homme. Et vous avez ici une belle tomographie qui vous montre un embryon à au stade E12, au jour embryonnaire 12. Et la derrière, on est ici de voir le cette structure qui est le cerveau antérieur, les vésicules céphalique qui deviendront le cortex. Alors, je vais essayer de vous passer le film. comme ça vous pouvez apprécier la la structure en trois dimensions. Par exemple, on peut utiliser la souris pour euh analyser des défauts de migration. Ici, c'est une mutation dans un gène qui code pour la double cortine, dont on sait que chez l'homme, elle est impliquée dans la lissencéphalie. Euh voici à travail du laboratoire non encore publié où la mutation d'un gène induit une microcéphalie chez la souris. Alors, nous allons bénéficier parce que je vais vous parler maintenant de migration neuronale, d'une découverte qui a été faite il y a quelques années, qui est la protéine fluorescente verte qui a été clonée à partir d'une méduse. Et qui peut être exprimé de façon spécifique et conditionnelle euh dans le cerveau par exemple, de la souris et ça permet par exemple de tracer certains types neuronaux. Donc nous avons nous allons utiliser des souris transgéniques, mais également une technique qui nous permet de moduler de façon spatiale et temporelle l'expression des gènes dans le cerveau des embryons murins pendant la gestation. Il s'agit de l'électroporation in utéro. Et donc l'idée des est d'injecter des des plasmides pour permettre de moduler par exemple, surexprimer certains gènes en présence de la GFP, ce qui nous permet ensuite de tracer les cellules qui ont été électroporées transfectées. Voyez ici par exemple, une électroporation qui est réalisée au jour E14. 3 jours plus tard, vous avez ici un cerveau qui est disséqué et qui vous montre le patch de cellules vertes qui est la région qui a été électroporée. Une coupe à travers cette région vous montre le cortex et la corde de cellules qui a été ciblée. Et donc il est possible de surexprimer des gènes, mais également d'induire un une réduction de l'expression de certains gènes par ARN interférence. Avec cette technique, nous sommes capables d'analyser le mode de migration des neurones de projection ou des interneurones.
[10:44]Je vais essayer de nouveau de vous montrer Voilà, donc ceci, c'est la migration radiaire des neurones de projection. Vous avez les cellules souches qui se trouvent ici et vous allez vous rendre compte que la migration euh des des interneurones est un peu différente. Donc je vais euh diviser l'exposé en deux parties expérimentales, la première, donc ce sont des des des recherches qui ont été menées au sein de mon laboratoire à trait à la régulation de la migration des interneurones corticaux et puis je vous présenterai une autre recherche, euh, qui concerne euh le contrôle moléculaire de la migration des neurones de projection, les neurones excitateurs. Mais démarrons d'abord avec les les interneurones. Pour rappel, ces interneurones sont générés, produits dans la partie ventrale du cerveau antérieur pendant le développement. On parle d'éminence ganglionnaire médiane et caudale.
[11:42]Vous voyez que les chemins de migration sont très complexes et sont remodelés de façon dynamique pendant le développement cortical. Sur un même plan euh de migration tangentielle, vous pouvez observer une dispersion multidirectionnelle de ces interneurones de façon à peupler de façon relativement homogène certaines régions du cortex. Alors cette migration euh d'interneurones dépend d'une collaboration euh entre la dialogue entre des signaux environnementaux et des régulateurs intrinsèques. En effet, parmi les signaux environnementaux, il y a des euh des molécules chimioattractantes ou chimiorepulsives qui finalement dessinent ces chemins de migration. Les régulateurs intrinsèques, et la liste n'est pas exhaustive, sont importants pour contrôler le comportement dynamique de ces interneurones. Et j'y reviendrai et la plupart d'entre eux influence de façon directe ou indirecte le remodelage du cytosquelette de microtubules et d'actine. Laissez-moi vous parler de de P27. P27, comme vous le savez probablement, est une petite protéine qui promeut la sortie de cycle en inhibant l'activité de CDK, CDK2 en l'occurrence. Euh P27 fait partie d'une famille, la famille Sip qui comportant également P21 et P57. Nous avons après quelques années que P27 possédait des fonctions indépendantes de la régulation du cycle. En effet, nous montrons que P27 est exprimé dans des cellules postmitotiques après la sortie du cycle. Et comme vous pouvez le constater sur cette image, voici une immunohistochimie sur un cerveau d'une souris rapporteuse, c'est un embryon à E14, rapporteuse parce qu'elle exprime la GFP dans tous les interneurones. En rouge, P27 est exprimé dans le noyau de ces cellules, mais également dans le cytoplasme, peut-être un peu difficile à voir d'où vous êtes. Mais ce qui est important, c'est que ces cellules ne prolifèrent pas, elles sont en train de migrer et de s'installer dans le cortex. Ça suggère que P27 puisse jouer des rôles indépendants de la régulation du cycle et peut-être être impliqué dans le contrôle de la migration. Cette hypothèse, nous avons décidé de la tester en utilisant différentes approches expérimentales et je vous parlerai d'une seule approche. C'est une approche transgénique. En fait, nous utilisons euh des croisements de souris nous permettant de d'invalider de façon conditionnelle P27 dans les interneurones postmitotiques. En croisant des souris pour lesquelles le locus de P27 est loxé avec des souris rapporteuses qui expriment la créa fusionnée à la GFP, ce qui nous permet de tracer les neurones en même temps. Euh, la dépendance d'une séquence régulatrice euh de gènes impliqués, enfin importante pour le développement des des interneurones, nous pouvons suivre ainsi euh des cellules postmitotiques, des interneurones invalidées pour l'expression de P27. Et vous avez ici euh la la démonstration que le modèle fonctionne puisque euh nous observons une expression mutuellement exclusive de P27 et de la GFP euh et donc de la créa. Avec ce modèle, nous avons étudié la migration des interneurones. Alors, voici un dessin représentant une demi-section coronale à travers le le cortex en plutôt j'aurais-je dire le le cerveau antérieur de la souris embryonnaire à E12. Et nous sommes à E12, moment auquel la première vague d'interneurones pénètre dans le cortex. Vous avez ici le cortex, la partie ventrale et cette frontière qui est appelée frontière corticos-triatale. Ou palial, subpalial. Et nous mesurons donc euh le pourcentage de cellules qui passe dans le cortex et qui proviennent euh des éminences ganglionnaire. Vous voyez qu'en l'absence de P27, il y a une réduction significative du nombre de cellules qui pénètre le cortex et ceci à différentes régions rostrocaudal. Cette réduction du nombre de cellules s'accompagne en fait d'une diminution de la vitesse de déplacement des interneurones dépourvue d'expression de P27. Alors nous avons tenté de mieux comprendre pourquoi cette réduction de vitesse avait lieu en l'absence de P27. Je vous rappelle que l'interneurone migre de façon tout à fait particulière euh et implique des changements morphologiques extrêmement importants. Donc vous avez ici la la direction de migration, euh le soma, le noyau. Une petite région cytoplasmique qui s'amplifie qui migre dans le processus de guidage euh dans les cas dans laquelle on retrouve également euh les centriolles et l'appareil de Golgi. S'ensuit ensuite une translocation extrêmement rapide du noyau. On parle de nucléokinèse et d'un branchement euh du cône de croissance pour former des branches euh dichotomiques qui s'éliminent progressivement et se reforment pour diriger la cellule dans le parenchyme cortical. Et donc voici un un film vous montrant
[17:58]vous montrant le le déplacement de ces de ces interneurones dans le parenchyme cortical. Vous voyez que ce schéma représente la la réalité. Pour résumer, lorsque P27 n'est pas exprimé dans ces neurones, nous observons une augmentation de la fréquence de la nucléokinèse. Donc ce cette translocation rapide du noyau vers le la partie cytoplasmique ici. Mais cette fréquence de nucléokinèse s'accompagne également d'une réduction de la distance de déplacement du noyau. Nous observons également un problème de branchement du processus de guidage, il y a une augmentation de son branchement et les branches qui en résultent sont extrêmement instables. Donc finalement, la cellule invalidée pour P27 nous apparaît comme étant plus petite et extrêmement branchée. Ceci explique probablement la moins bonne efficacité de migration de ces interneurones lorsque P27 n'est pas exprimé dans ces cellules. Nous avons démontré que il y avait une colocalisation intéressante entre P27 et une petite GTPase appelée RoA, que vous voyez ici. Par immunoprécipitation, nous montrons également une interaction physique entre ces protéines. Et en fait, nous avons pu observer que l'interaction de P27 sur cette petite GTPase connue pour réguler la motilité, empêchait l'activation de cette GTPase par ces F. Et ceci est montré par cette immunoprécipitation où vous voyez une bande plus importante dans du tissu lorsque P27 n'est pas exprimé. Cette bande correspondant à la forme activée de RoA dans le système.
[20:25]Donc nous pensons que P27 exerce un rôle de frein sur la transduction d'une voie de signalisation impliquant RoA et aboutissant à la régulation de la nucléokinèse et du branchement dynamique de ces cellules. En fait, il s'agit d'un contrôle fin de l'activité de la myosine 2. La myosine 2 est un euh est une protéine, est une myosine non musculaire. euh qui se déplace sur les filaments d'actine et qui est importante pour les contractions d'actomyosine. Ces contractions que vous voyez en bleu sont importantes elles-mêmes pour euh pousser le noyau dans le processus de guidage durant la nucléokinèse.
[21:23]Alors la myosine 2 est composée de différentes sous-unités, une euh sous-unité lourde et deux petites sous-unités, dont une sous-unité de régulation qui doit être phosphorylées pour activer le complexe. Il s'agit de la MLC2, la chaîne légère de type 2. Alors, vous pouvez voir que sa distribution est assez homogène dans l'interneurone, il s'agit d'un interneurone. Ce qui suggère que le la myosine est localisée partout, mais son activation qu'on peut observer par la phosphorylation, enfin en tout cas le le marquage de la forme phosphorylée de la chaîne légère est localisé à l'arrière du noyau et au niveau des branchements nouvellement formés. Exactement là où on s'attend à avoir un problème puisque c'est la nucléokinèse et le branchement qui sont altérées lorsque P27 n'est pas exprimé dans ces neurones. Et ces Western blot vous montrent en fait que lorsque P27 n'est pas exprimé, dans du tissu provenant des éminences ganglionnaires, et bien nous avons une augmentation très significative de la phosphorylation de la chaîne légère qui signe une augmentation de l'activité de l'actomyosine et donc des contractions d'actomyosine qui ont lieu pendant le mouvement. Alors, il nous est malheureusement impossible de suivre en direct par time-lapse la l'activité de la myosine 2. Mais nous pouvons le faire de façon indirecte. En utilisant une sonde appelée Utrop GFP. Cette sonde est basée sur un élément de l'utrophine qui se fixe à l'actine filamenteuse, fusionnée à la GFP, ce qui nous permet en fait de localiser les régions où l'actine filamenteuse se condense. Et qui reflète les régions de contractilité. Euh vous pouvez voir ici euh la colocalisation de ces régions avec euh les régions où la myosine 2 est active. Alors, à l'aide de cette sonde et à l'aide de la microscopie confocale et du time-lapse, nous pouvons mesurer la condensation de l'actine en live dans la cellule qui va euh subir une nucléocinèse. La GFP est pseudocolorisée en feu, en couleur de feu. Cela nous permet non seulement de de voir où se trouve le signal mais également de mesurer son intensité. Et donc vous avez ici une cellule, il s'agit d'un interneurone type avec la distribution en live de cette contractilité.
[24:50]Vous voyez qu'il y a une activité extrêmement importante dans le cône de croissance qui est en train de former les branches, mais également à l'arrière du noyau, et ceci est important pour pousser le noyau pendant la nucléocinèse. Cette séquence d'activation est conservée chez le mutant dans la dans la cellule dépourvue de mutation de P27. Mais le temps d'activation et l'intensité de l'activation est beaucoup plus importante, que ça soit derrière le noyau, et ceci est mesuré par cet histogramme. Mais également dans le cône de croissance qui va former les branches, ce que je ne vous montre pas ici. Alors la séquence est conservée.
[25:49]Vous voyez une activation beaucoup plus longue. Également, je l'ai décrit tout à l'heure, des nucléokinèses plus importantes, donc une fréquence de nucléokinèse plus importante avec une réduction de la distance de déplacement. Donc nous pensons que en l'absence de P27, la voie de signalisation impliquant RoA et la myosine 2 est dérégulée. Et nous avons donc une hyperactivation de la myosine 2 qui contribue au défaut de contractilité que je vous ai montré et qui sous-tend probablement le problème de migration. La l'étape suivante était de le démontrer, ce que nous avons fait par microscopie confocale et enregistrement en temps réel, time-lapse. Nous avons décidé de tenter de corriger les défauts que je viens d'écrire, nucléocinèse et branchement en traitant les cultures d'interneurone dépourvu d'expression de P27 avec différents bloqueurs pharmacologiques. Ou à l'aide d'une approche génétique. Pour résumer, nous voyons que ces approches permettent de restaurer la fréquence de nucléocinèse, ainsi que la formation de nouvelles branches neuritiques. Cependant, nous voyons que l'extension des neurites reste affectée. Il semble donc que P27 soit important pour contrôler la nucléocinèse et le branchement via cette voie de signalisation, mais que P27 agissent via une autre voie de régulation pour permettre l'extension des neurites pendant le mouvement. Et pour résumer également, nous avons décidé de regarder les microtubules parce que nous savons que les microtubules doivent polymériser et se stabiliser pour permettre l'extension des neurites. Donc l'hypothèse a été de voir enfin de de de postuler que P27 devait être capable de contrôler d'une certaine manière la dynamique des microtubules. Pour tester cette hypothèse, nous avons réalisé une analyse de comètes. Alors, je vous explique, nous avons euh des cellules qui sont wild-type ou dépourvues d'expression de P27 que nous transfectons avec une construction de type EB3 GFP. IB3 étant une protéine qui se fixe de façon transitoire, très transitoire à l'extrémité croissante des microtubules, l'extrémité plus. Et qui est fusionnée à la GFP, ce qui nous permet de suivre la croissance des microtubules en live. Et voici un film qui vous montre le déplacement de ces comètes.
[29:08]La mesure de vitesse du déplacement de ces comètes reflète directement le taux de polymérisation des microtubules.
[29:21]Et vous voyez que lorsqu'on réalise cette expérience dans des cellules dépourvues d'expression de P27, nous avons une réduction significative euh de la vitesse et donc du taux de polymérisation des microtubules. Défaut qui peut être corrigé en réexprimant P27 dans ces cellules qui étaient dépourvues de P27. Nous montrons également par microscopie en super résolution, ce qui nous permet d'atteindre des échelles de l'ordre de des dizaines de nanomètres, ça doit être 100 nanomètres ici. Vous avez ici un un microtubule unique qui est décoré par P27. Ceci suggère une interaction entre les protéines que nous démontrons par immunoprécipitation. Mais également par cossédimentation in vitro et je ne vous donnerai pas le détail, ce qui nous permet en fait de dire et c'est la première fois que cela est montré, que P27 est également une protéine directement associée aux microtubules, une map euh microtubule protein. Ces protéines sont connues comme étant importantes pour contrôler les les microtubules. Et nous avons ensuite décidé de déterminer quels étaient les domaines impliqués euh dans le contrôle de l'interaction et de la polymérisation des microtubules par P27. Et nous avons identifié ce domaine euh riche en proline qui lorsqu'il est muté, et bien, empêche la polymérisation. Et je vous montre ça ici. Donc vous vous souvenez de cette expérience où nous mesurons le taux de polymérisation. Il est inférieur lorsque P27 n'est pas exprimé, il est corrigé dans ces cellules lock-out lorsqu'on réintroduit la forme pleine longueur de P27, mais pas celle dépourvue de ces quatre prolines qui ont été mutées et remplacées par des alanines. Cela suggère que ce domaine est nécessaire pour permettre à P27 de promouvoir la polymérisation des microtubules. Donc je vous ai parlé de l'extension de neurite et nous avons postulé à l'époque que P27 était capable probablement de contrôler la dynamique des microtubules. Alors est-ce que cela est nécessaire pour l'extension des neurites ? Vous avez ici un un interneurone avec des neurites de différents ordres. Les résultats sont les mêmes pour tous les ordres. Donc je vais me consacrer à à vous expliquer ce qui se passe au premier ordre.
[32:29]Donc vous voyez ici sur cet histogramme, en noir c'est la valeur de la longueur du neurite primaire dans en condition de contrôle. En rouge, vous voyez le défaut significatif lorsque P27 n'est pas exprimé, et euh ce défaut peut être corrigé uniquement par expression de forme euh de P27 qui exprime ce domaine enrichi en proline. Donc, ceci est la démonstration que P27 contrôle l'extension neuronique via ce petit domaine euh moléculaire. Alors l'extension neuronique est-elle importante pour la migration ? Euh et ceci est la dernière expérience pour pour cette partie. Euh nous avons décidé de tenter de restaurer la migration des interneurones lorsque P27 n'était pas exprimé, en réexprimant différentes formes de P27, et notamment celle qui n'était plus capable soit d'interagir avec l'actomyosine, soit d'interagir avec les microtubules. Donc vous avez ici le type d'expérience que nous avons réalisé, il s'agit de tranches de culture organotypique. Nous injectons et électroporons les interneurones avant leur sortie euh du du du cerveau euh ventral. Et nous mesurons leur migration et leur pénétration dans le cortex.
[34:15]Donc, vous avez ici, par exemple, euh une demi-coupe de à travers le cerveau antérieur euh de d'embryon wild-type, pardon. Nous injectons la GFP, 3 jours plus tard, vous voyez que ces interneurones colonisent euh le cortex. Ce n'est pas le cas lorsque de la GFP est électroporée tant euh des mutants P27.
[34:52]Alors, vous voyez que et c'est cette bar-ci, vous voyez que par rapport au défaut, on peut restaurer le défaut en électroporant P27, en remettant du P27 dans des tranches qui sont dépourvues de P27. Ce qui est intéressant, c'est que des formes mutantes incapables, soit d'interagir avec l'actomyosine, soit d'interagir avec les microtubules, ne restent que partiellement l'activité. Et donc, ceci suggère que P27 est un chef d'orchestre important pour le contrôle de la migration des interneurones.
[35:42]Et ceci en agissant sur deux voies de mécanisme de moléculaire indépendante. Une première voie via un domaine que nous avons euh répertorié en en ces terminales qui euh contrôle la transduction à travers la voie de signalisation RoA, Myosine 2, qui est importante pour le contrôle de la nucléokinèse mais également des étapes initiales du branchement dynamique. Et nous montrons et c'est le comme message de cette partie que P27 est également une protéine associée aux microtubules qui promeut la polymérisation des microtubules. Et ceci est important pour l'extension dynamique des des neurites. Et donc ces deux fonctions sont importantes pour permettre une migration ad hoc des interneurones dans le cortex cérébral. Je vais ensuite passer euh à l'explication d'une autre recherche menée au sein du laboratoire qui a trait à la migration des neurones de projection. Les neurones de projection, comme je vous l'ai dit, sont nés dorsalement à partir de progéniteurs et de cellules souches. qui migrent en vague pour s'installer de façon inside out dans le cortex, six couches. Durant cette migration, ces neurones de projection subissent également des morph des modifications morphologiques importantes. Vous avez par exemple cette étape qui est cruciale qui est l'étape multipolaire. Il s'ensuit une repolarisation et donc les cellules deviennent bipolaires, ce qui leur permet de rentrer en locomotion sur les fibres de la glie radiaire et de migrer.
[46:07]Je pense que c'est ça n'a jamais été euh étudié euh chez chez l'homme, c'est et je ne pense pas qu'il y a des modèles animaux qui qui ont été entrepris pour poser cette question qui est intéressante, je pense. Monsieur le Febvre. Juste une question sur P27 encore. P27 est aussi impliqué dans la prolifération cellulaire, notamment dans l'oreille, qui est un domaine que je connais. Et dans l'oreille, quand on P27, on augmente drastiquement le nombre de cellules ciliées. Euh, une des questions, il y a deux questions là en dessous. Est-ce que cette modification et cette prolifération possible est aussi par l'intermédiaire d'un d'une interaction avec les microtubules ou les ou les systèmes qui jouent un rôle dans les mitoses. Ça c'est la première chose, première question. Deuxième question, est-ce que euh on observe aussi ce genre de choses lorsqu'on bloque P27 dans un cortex cérébral ? Est-ce qu'il y a une augmentation des mitoses aussi ? Alors ici, j'ai j'ai vraiment décrit les fonctions postmitotiques de P27, mais évidemment, comme vous le soulignez, P27 est un régulateur du cycle. Et donc lorsqu'on module l'expression de P27 dans les progéniteurs du cortex, on altère leur prolifération. C'est un frein à la prolifération et donc évidemment, on augmente le nombre de de de mitose. C'est intéressant, vous soulignez le fait que P27 a aussi un effet euh dans l'oreille. Euh alors, est-ce que c'est un effet lié à à sa capacité à réguler la la prolifération ou un autre effet euh sur par exemple les microtubules, comme vous le soulignez. C'est une question intéressante parce que nous nous pensons que que P27 est est un peu une protéine qui sert à plus à plusieurs fonctions. Et euh dans le cadre de l'oreille, c'est pas clair, je pense actuellement de savoir si c'est la dérégulation de la prolifération ou l'activité que P27 pourrait avoir envers certains substrats qui qui modifieraient leur spécification. Alors, pour revenir aux microtubules, euh P27, nous montrons qu'il est effectivement capable de s'associer aux microtubules dans les cellules postmitotiques. Et euh nous avons donc décidé de réanalyser, c'est ce que nous faisons actuellement, le dogme par lequel P27 contrôle la prolifération uniquement via les CDK. Nous pensons que par exemple, la séparation des microtubules pourrait être dépendante de la régulation de P27.
[49:25]Mais il montre que lorsque P27 n'est pas exprimé, euh ce n'est pas la quiescence qui est altérée, mais plutôt le comportement des progéniteurs intermédiaires. Il y a donc une surprolifération de ces progéniteurs intermédiaires.